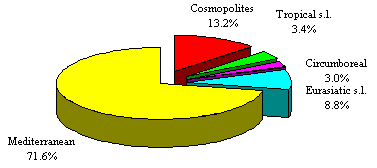English |
Discussione |
|||||||
![]()
Le ricerche condotte nella parte montana e collinare del bacino idrografico del Rio Santa Lucia hanno permesso di censire 669 taxa di cui 628 di rango specifico, 35 sottospecifico, 2 varietale e 4 ibridi, afferenti a 364 generi e 101 famiglie (tab. 4). Le Dicotyledones con 70 famiglie, 266 generi e 486 entit� sono risultate dominanti rispetto agli altri gruppi sistematici.
FAMIGLIE
GENERI
SPECIE
SUBSPECIE
VARIETA'
IBRIDI
Pteridophyta 13
16
23
2
-
-
Gymnospermae 3
3
4
-
-
-
Dicotyledones 70
266
456
28
2
-
Monocotyledones 15
79
146
5
-
3
Totale 101
364
629
35
2
3
Tab. 4. Taxa flora Rio Santa Lucia.
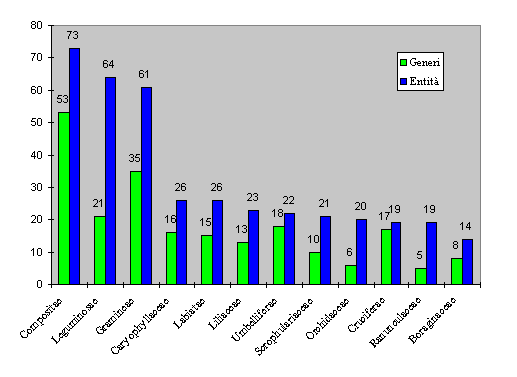
Tra le famiglie con il maggior numero di entit� (fig. 2 e tab. 5) al primo posto troviamo le Compositae (73), seguite dalle Leguminosae (64) e dalle Gramineae (61). Interessante appare il dato delle Umbelliferae e delle Cruciferae che presentano un numero di generi (rispettivamente 18 e 17), prossimo a quello delle entit� (22 e 19).
Fig. 2. Famiglie con pi� generi ed entit�.
Famiglie Generi
Specie
Subspecie
Ibridi
Totale
Compositae 53
70
3
-
73
Leguminosae 21
60
4
-
64
Gramineae 35
60
1
-
61
Caryophyllaceae 16
25
1
-
26
Labiatae 15
23
3
-
26
Liliaceae 13
23
-
-
23
Umbelliferae 18
19
3
-
22
Scrophulariaceae 10
21
-
-
21
Orchidaceae 6
14
3
3
20
Cruciferae 17
18
1
-
19
Ranunculaceae 5
17
2
-
19
Boraginaceae 8
14
-
-
14
Tab. 5. Famiglie con pi� taxa.
Relativamente alla ricchezza floristica, nella tab. 6 si � messo a confronto il territorio studiato con le vicine aree di Pixinamanna (Arrigoni 1964), Pantaleo-Gutturu Mannu-Punta Maxia (Camarda & al. 1993), Monte Tamara (Ballero & al. l.c.) e Monte Arcosu (Mossa & al. 1996). Relativamente alla flora di Pixinamanna non sono stati considerati i taxa di rango inferiore a quello sottospecifico e ci� ha portato a una riduzione delle entit� da 552 a 467. Dalla comparazione delle diverse flore risulta che il bacino idrografico del Rio Santa Lucia � floristicamente pi� povero rispetto a tutte le altre aree eccezion fatta per quella di Pantaleo-Gutturu Mannu-Punta Maxia. Tali dati sono giustificati dalla notevole differenza di superficie, dalla natura dei substrati e dalla relativa omogeneit� del territorio esaminato rispetto alle aree di Monte Tamara, Monte Arcosu e Pixinamanna. L'unica zona effettivamente comparabile per superficie e omogeneit� territoriale risulta infatti quella di Pantaleo-Gutturu Mannu-Punta Maxia, che appare notevolmente pi� povera sia in termini strettamente numerici che di rapporto con la superficie.
FLORA Area (Kmq)
Entit�
Entit�/Kmq
Generi
Gen./Kmq
Famiglie
Fam./Kmq
Rio Santa Lucia 73
669
9.2
364
5.0
101
1.4
Monte Tamara (BALLERO & al. op. cit.) 25
472
18.9
294
11.8
78
3.1
Monte Arcosu (MOSSA & al. 1996) 32
520
16.3
303
9.5
90
2.8
Pixinamanna (ARRIGONI 1964) 40
467
11.7
269
6.7
n.s.
-
Pantaleo (CAMARDA & al. 1993) 120
593
4.9
338
2.8
90
0.8
Tab. 6. Ricchezza floristica.
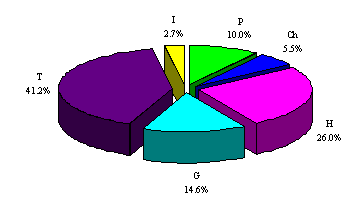
I dati dello spettro biologico (fig. 3) confermano essenzialmente la mediterraneit� dell’area (T=41.2%) e l’elevato grado di ricoprimento boschivo (P=10%). L’alta percentuale di geofite (G=14.6%) appare legata all’uso antropico del territorio, in particolar modo alla pratica degli incendi e alle attivit� di tipo silvo-pastorale. Significativa la percentuale di idrofite (I=2.7%), localizzate essenzialmente lungo i torrenti e presso le sorgenti.
Fig. 3. Spettro biologico della flora del bacino idrografico del Rio Santa Lucia.
Dalla comparazione dello spettro biologico (tab. 7) con quello della Sardegna (Bocchieri 1995) non emergono particolari discordanze, si evidenziano solo differenze per i valori delle terofite con la flora di Pixinamanna (Arrigoni 1964) e di Pantaleo-Gutturu Mannu-Punta Maxia (Camarda & al. 1993). I valori percentuali delle terofite rilevati per tali flore risultano significativamente superiori (10.8 e 7 punti %), senza che vi siano importanti giustificazioni paesaggistiche se non quelle della esposizione a mare per l’area di Pixinamanna e del probabile inserimento di aree agricole per quella di Pantaleo-Gutturu Mannu-Panta Maxia. Relativamente ai recenti lavori realizzati per il Monte Tamara e Arcosu, dalla comparazione con la flora del Rio Santa Lucia, i valori rilevati appaiono in linea eccezion fatta per le idrofite. Ci� � spiegabile con la natura geomorfologica e geologica dei due sistemi. Entrambi presentano infatti pochissimi corsi d'acqua e sorgenti, il Monte Tamara risulta inoltre costituito da rocce di natura calcarea che presentano anche fenomeni di carsismo di profondit�.
P
Ch
H
G
T
I
Rio Santa Lucia 10.0
5.5
26.0
14.6
41.2
2.7
Pixinamanna (Arrigoni 1964) 9.0
5.0
19.0
15.0
52.0
0.0
Pantaleo (Camarda & al. 1993) 9.3
3.7
26.7
11.4
48.2
0.7
M. Tamara (Ballero & al. op. cit.) 10.0
5.0
26.0
14.0
45.0
0.0
M. Arcosu (Mossa & al. 1996) 10.4
5.0
25.6
14.0
43.6
1.4
Sardegna (Bocchieri, op. cit.) 8.8
8.1
28.1
12.1
39.9
3.0
Tab. 7. Spettri biologici comparati.
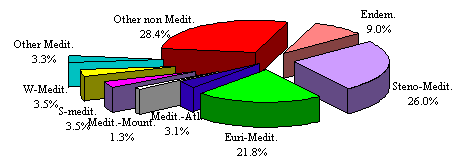
Per gli aspetti corologici, nella fig. 4 e nella tab. 8 vengono riportati lo spettro con le categorie corologiche raggruppate in macroforme affini per ottenere un confronto pi� immediato. Il secondo spettro (fig. 5 e tab. 9) rappresenta invece gli elementi mediterranei principali, mentre il terzo (fig. 6 e tab. 10) mette in evidenza tutti i subelementi mediterranei secondo un criterio biogeografico e cardinale. Dagli spettri cos� realizzati risultano la dominanza delle specie mediterranee (71.6%) e in particolare quella degli elementi stenomediterranei (26%), eurimediterranei (21.8%) ed endemici (9%). La componente mediterraneo-occidentale (3.6%), quella sud-mediterranea (3.4%) e quella mediterraneo-atlantica (3.1), appaiono importanti al fine dell'identificazione del baricentro dell’area studiata.
Fig. 4. Spettro corologico generale.
TIPO COROLOGICO n. taxa
%
Cosmopolite 88
13.2
Tropicali s.l. 23
3.4
Circumboreali 20
3.0
Eurasiatiche s.l. 59
8.8
Mediterraneanee 479
71.6
Totale 669
100.0
Tab. 8. Tipi corologici generali.
Fig. 5. Spettro corologico degli elementi mediterranei principali.
TIPO COROLOGICO n. taxa
%
Endem. 60
9.0
Steno-Medit. 174
26.0
Euri-Medit. 147
21.8
Medit.-Atl. 21
3.1
Medit.-Mount. 9
1.3
S-medit. 23
3.5
W-Medit. 23
3.5
Altre Medit. 22
3.3
Altre non Medit. 190
28.4
Total 669
100.0
Tab. 9. Main Mediterranean chorological types.
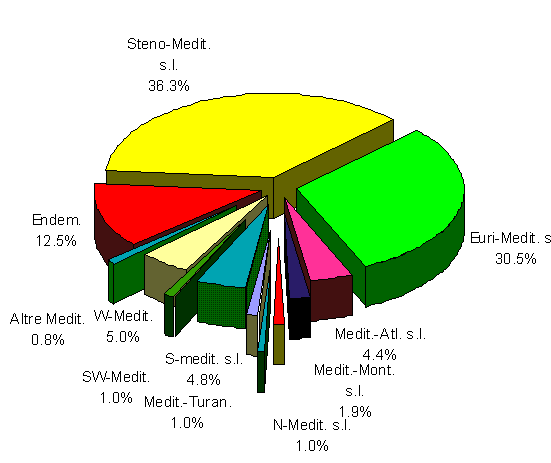
Fig. 6. Spettro corologico dei subelementi mediterranei.
TIPO COROLOGICO n. taxa
%
Endem. 60
12.50
Steno-Medit. s.s. 127
W-Steno-Medit. 30
Steno-Medit.-Macarones. 9
Steno-Medit.-Turan. 8
Steno-Medit. s.l. 174
36.3
Euri-Medit. s.s. 127
Euri-Medit.-Turan. 10
W-Euri-Medit. 6
Euri.-Medit.-Macarones. 4
Euri-Medit. s.l. 147
30.5
Medit.-Atl. s.s. 15
Submedit.-Subatl. 6
Medit.-Atl. s.l. 21
4.4
Medit.-Mount. s.s. 6
W-Medit.-Mount. 3
Medit.-Mount. s.l. 9
1.9
TIPO COROLOGICO n. taxa
%
N-Medit. s.s. 3
NE-Medit. 1
NW-Medit. 1
N-Medit. s.l. 5
1.0
E-Medit. s.s. 2
E-Medit.-Turan. 1
E-Medit. s.l. 3
0.6
Medit.-Turan. 5
1.0
S-Medit. s.s. 20
S-Medit.-Turan. 3
S-Medit. s.l. 23
4.8
SW-Medit. 5
1.0
W-Medit. 19
W-Medit.-Macarones. 4
W-Medit. 23
5.0
Other Medit. 4
0.8
Total Medit. 479
100.0
Tab. 10. Subelementi mediterranei.
Lo spettro delle entit� endemiche (60 taxa, di cui 51 di rango specifico, 7 sottospecifico e 2 ibridi) � stato realizzato differenziando la componente sarda da quella sardo-corsa e le altre a pi� ampia distribuzione (fig. 7 e tab. 11). Le entit� a gravitazione tirrenica e quelle presenti anche sulle coste francesi (Ga) e isole Hy�res (H), secondo quanto proposto da Arrigoni & Di Tommaso (1991), sono state inserite nelle categorie delle endemiche tirrenico insulari, tirreniche e del mediterraneo occidentale. Il grafico mostra una netta dominanza delle endemiche sardo-corse (31.7%) e di quelle sarde (21.7%), che unitamente raggiungono il 53.4% del totale. Il dato delle sardo-corse e delle sardo-corse-arcipelago toscano (16.7%) risulta cos� elevato per effetto del substrato di natura silicea che tende a dominare le morfologie delle zone cacuminali, delle pareti rocciose e delle aree poste al di sopra dei 400-600 m di quota.
Fig. 7. Spettro corologico della componente endemica.
n. taxa |
% |
|
| Sardegna | 13 |
21.7 |
| Sardegna-Corsica | 19 |
31.7 |
| Sardegna-Corsica-Arcip. Toscano | 10 |
16.7 |
| Sardegna-Corsica-Arcip. Toscano-Baleari | 6 |
10.0 |
| Endem. tirrenico insulari (sensu Arrigoni & al. l.c.) | 4 |
6.7 |
| Endem. Tirreniche (sensu Arrigoni & al. l.c.) | 3 |
5.0 |
| Endem. Mediterraneo-occid. (sensu Arrigoni & al. l.c.) | 5 |
8.3 |
| Totale | 60 |
100.0 |
Tab. 11. Numero e percentuale di endemiche.
La componente endemica (tab. 12) ed in particolare i taxa esclusivi Armeria sulcitana Arrigoni, Genista valsecchiae Brullo & De Marco ed Helichrysum montelinasanum E. Schmid evidenziano l'autonomia floristica del settore, confermando quanto gi� posto in rilievo da Mossa & al. (1996).
Il ritrovamento di Borago pygmaea (DC.) Chater & Greuter, Galium corsicum Sprengel, Genista aetnensis (Biv.) DC., Genista valsecchiae Brullo & De Marco, Linaria arcusangeli Atzei & Camarda, Ophrys x maremmae O. & E. Danesch nsubsp. woodii Corrias e di Orchis x penzigiana Camus nsubsp. sardoa Scrugli & Grasso, contribuisce a meglio definire l'areale e l'ecologia di tali entit�.
In particolare, il rinvenimento di Borago pygmaea (DC.) Chater & Greuter nel Canale di Sa Senna Manna ed in quello di Longufresu, conferma il dato bibliografico riportato da Valsecchi (l.c.) relativamente a un exsiccata della zona di Capoterra, presente nell'erbario di Cagliari e privo di data e raccoglitore.
Per quanto riguarda Galium corsicum Sprengel, si tratta della prima segnalazione per il Sulcis e della seconda per la Sardegna meridionale, precedentemente era stato infatti ritrovato solo sul Monte Linas da Angiolino e Chiappini (1983).
Genista aetnensis (Biv.) DC. sino ad ora era stata segnalata solo per la localit� Is Cannoneris (Camarda & al. 1993), mentre Genista valsecchiae Brullo & De Marco ritenuta costiera in quanto segnalata esclusivamente per le coste sud-occidentali (Brullo & De Marco 1996).
Il ritrovamento di Linaria arcusangeli Atzei & Camarda sia sul Monte Arcosu che sul Monte Lattias, amplia ai monti sulcitani l'areale di questa specie, in quanto segnalata sino ad oggi solo per l'Arco dell'Angelo (Atzei & Camarda 1984, Camarda 1985) e per il Rio Cannas (BALLERO, 1988).
Relativamente a Ophrys x maremmae O. & E. Danesch nsubsp. woodii Corrias e Orchis x penzigiana Camus nsubsp. sardoa Scrugli & Grasso, va detto che si tratta della prima segnalazione per il Sulcis e che di entrambe le entit� � stato rinvenuto un solo esemplare.
Interessanti anche i dati che confermano la presenza di rari endemismi quali Genista morisii Colla, Mentha requienii Bentham, Ophrys holoserica (Burm.) Greuter subsp. chestermanii Wood, Orchis mascula (L.) L. subsp. ichnusae Corrias e Soleirolia soleirolii (Req.) Dandy.
Tra le entit� endemiche, sono state inserite anche Dipsacus ferox Loisel. in accordo con quanto proposto da Bocchieri & al. (l.c.) e Helichrysum italicum (Roth) Don subsp. microphyllum (Willd.) Nyman secondo quanto proposto da Biondi & al. (l.c.).
Per quanto riguarda invece Serapias nurrica Corrias, va evidenziato che non � stata inserita tra le entit� endemiche sulla base dei recenti ritrovamenti nel sud del Portogallo (Salkowski 1993) e delle ricerche di carattere tassonomico e fitogeografico (Scrugli 1997). Sulla base di tali studi e secondo quanto proposto da Scrugli (1997), si � perci� ritenuto pi� opportuno considerare tale specie come una stenomediterranea occidentale.
ENTITA' AREALE Allium parciflorum Viv. Sa-Co Arenaria balearica L. Sa-Co-AT-Bl Aristolochia rotunda L. subsp. insularis (Nardi & Arrigoni) Gamisans Sa-Co Aristolochia tyrrhena Nardi & Arrigoni Sa Armeria sulcitana Arrigoni Sa Arum pictum L. f. Sa-Co-AT-Bl Barbarea rupicola Moris Sa-Co Bellium bellidioides L. Sa-Co-Bl Bituminaria morisiana (Pign. & Metlesics) Greuter Sa-La Galite (Tn) Borago pygmaea (DC.) Chater & Greuter Sa-Co-AT Bryonia marmorata Petit Sa-Co Carex microcarpa Bertol. ex Moris Sa-Co-AT Crocus minimus DC. in R�dout� Sa-Co-AT Cymbalaria aequitriloba (Viv.) A. Chev. Sa-Co-AT-Bl Delphinium pictum Willd. Sa-Co-Bl-H Dianthus siculus C. Presl. Sa-Co-Si Dipsacus ferox Loisel. Sa-Co Euphorbia cupanii Guss. ex Bertol. Sa-Co-Si Euphorbia semiperfoliata Viv. Sa-Co Galium corsicum Sprengel Sa-Co Genista aetnensis (Biv.) DC. Sa-Si Genista corsica (Loisel.) DC. in Lam. & DC. Sa-Co Genista valsecchiae Brullo & De Marco Sa Genista morisii Colla Sa Helichrysum italicum (Roth) subsp. microphyllum (Willd.) Nyman Sa-Co-Bl Helichrysum montelinasanum E. Schmid Sa Hypericum hircinum L. Sa-Co-AT Leucanthemum flosculosum (L.) P. Giraud Sa-Co Linaria arcusangeli Atzei & Camarda Sa Mentha insularis Req. ex Gren. & Godr. Sa-Co-AT-Bl Mentha requienii Bentham Sa-Co-AT Mercurialis corsica Cosson Sa-Co Oenanthe lisae Moris Sa Ophrys holoserica (Burm.) Greuter subsp. chestermanii Wood Sa Ophrys morisii (Martelli) So� in Keller & al. Sa-Co Ophrys x maremmae O. & E. Danesch nsubsp. woodii Corrias Sa Orchis mascula (L.) L. subsp. ichnusae Corrias Sa Orchis x penzigiana Camus nsubsp. sardoa Scrugli & Grasso Sa Ornithogalum biflorum Jordan & Fourr. Sa-Co Orobanche rigens Loisel. Sa-Co Pancratium illyricum L. Sa-Co-AT Polygonum scoparium Req. ex Loisel. Sa-Co Ptilostemon casabonae (L.) Greuter Sa-Co-AT-H Ranunculus cordiger Viv. subsp. diffusus (Moris) Arrigoni Sa-Co Ranunculus revelieri Boreau Sa-Co-Ga Robertia taraxacoides (Loisel.) DC. Sa-Co-Si-It Romulea requieni Parl. Sa-Co-It Salix arrigoni Brullo Sa Saxifraga corsica Gren. & Godr. Sa-Co Scrophularia ramosissima Loisel. Sa-Co-Bl-Ga Scrophularia trifoliata L. Sa-Co-AT Seseli bocconi Guss. subsp. praecox Gamisans Sa-Co Silene nodulosa Viv. Sa-Co Soleirolia soleirolii (Req.) Dandy Sa-Co-AT-(Bl) Stachys corsica Pers. Sa-Co Stachys glutinosa L. Sa-Co-AT Teucrium marum L. Sa-Co-AT-(Bl)-H Urtica atrovirens Req. ex Loisel. Sa-Co-AT-(Bl)-It Verbascum conocarpum Moris Sa-Co-AT Viola corsica Nyman subsp. limbarae Merxm. & Lippert Sa Tab. 12. La componente endemica del Rio Santa Lucia.
Per quanto riguarda i taxa d’interesse fitogeografico, viene confermato il dato attinente il ritrovamento di Urginea fugax (Moris) Steinh. (Arrigoni 1964), Salix atrocinerea Brot. (Camarda & al. 1993) e Spiranthes aestivalis (Poiret in Lam.) L.C.M. Richard. (Marras & al. 1995).
Relativamente a Taxus baccata L., si evidenziano un secondo popolamento nel Canale di Senna Manna e la presenza di diversi esemplari isolati, sia sulle creste del Monte Lattias che nel Rio su Fundu.
Vengono segnalate, nuove per il Sulcis: Blechnum spicant (L.) Roth, Cneorum tricoccon L., Laurus nobilis L., Leucojum aestivum L. subsp. pulchellum (Salisb.) Briq., Lilium candidum L., Quercus x morisii Borz� e Scilla obtusifolia Poiret.
In particolare, riguardo a Blechnum spicant (L.) Roth va evidenziato che si tratta della terza segnalazione per la Sardegna e della stazione pi� meridionale, precedentemente era conosciuta infatti solo per il Gennargentu e il Limbara (Ferrarini & al. l.c.).
I popolamenti di Laurus nobilis L., per la posizione inaccessibile in cui si trovano e per le notevoli dimensioni degli esemplari, rappresentano sicuramente uno degli esempi relittuali di laurisilva pi� interessanti della Sardegna.
![]()